北京擎科生物科技股份有限公司品牌商
7 年
手机商铺
- NaN
- 0.5
- 0.5
- 1.5
- 0.5
北京擎科生物科技股份有限公司
入驻年限:7 年
- 联系人:
张楠
- 所在地区:
北京 大兴区
- 业务范围:
实验室仪器 / 设备、试剂、技术服务、细胞库 / 细胞培养、抗体、ELISA 试剂盒、耗材
- 经营模式:
生产厂商 科研机构
公司新闻/正文
文献分享|综述:下一代CRISPR-Cas技术和应用
4325 人阅读发布时间:2021-07-08 15:47

1.CRISPR-Cas基因编辑工具概述
CRISPR-Cas系统是用于裂解入侵核酸的原核适应性免疫机制。CRISPR-Cas系统的分类存在于不同种类的细菌和古细菌,它们的组成和作用机制不同。第1类CRISPR-Cas系统包含多蛋白效应复合物,第2类系统只有一个效应蛋白; CRISPR-Cas系统依赖于CRISPR RNA (crRNA),向导RNA (gRNA)指导和目标特异性杂交(图1),定位到PAM或PFS序列,Cas核酸酶切断目标核酸。因此,任何包含PAM或PFS的位点特异性切割都可以通过设计crRNA来实现。
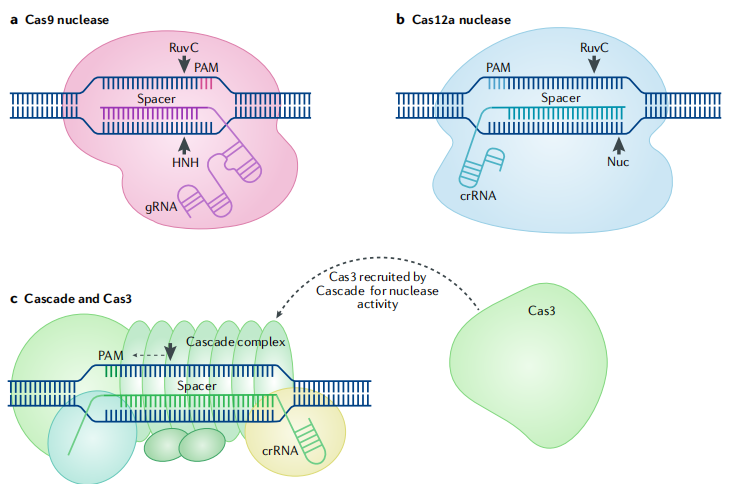
图1. CRISPR-Cas基因编辑工具概述
CRISPR-Cas系统是通过设计含有目标序列间隔的crRNA或gRNAs来结合特定序列。除了结合特定的核酸序列,这些蛋白质还具有核酸酶的功能,可用于编辑基因组。利用CRISPR-Cas的独特性质,如PAM的特异性、蛋白质大小和核酸酶活性,CRISPR-Cas的DNA靶向工具已被开发用于基因组编辑。Cas9属于二类CRISPR系统,SpCas9可用于哺乳动物细胞,是最常用的Cas9。在识别DNA后,SpCas9会产生双链断裂(图1a)。SpCas9的DNA靶向依赖于20个核苷酸长的间隔区和PAM 5ʹ-NGG (N代表任何核苷酸)。Cas9系统是双RNA引导的:crRNA靶向DNA,后者负责与Cas9形成复合物。PAM 5’-NGG的识别限制了SpCas9靶位点在人类基因组中的可用性,平均每8个碱基对中有一个靶位点。为了增加目标位点,产生了改变PAM特异性的变体(表1)。例如,PAM SpCas9变体,xCas9,识别5ʹ-NG, 5ʹ-GAA和5ʹ-GAT PAM序列。
表1. Cas9变体具有改变的原间隔子邻近基序和靶向特异性
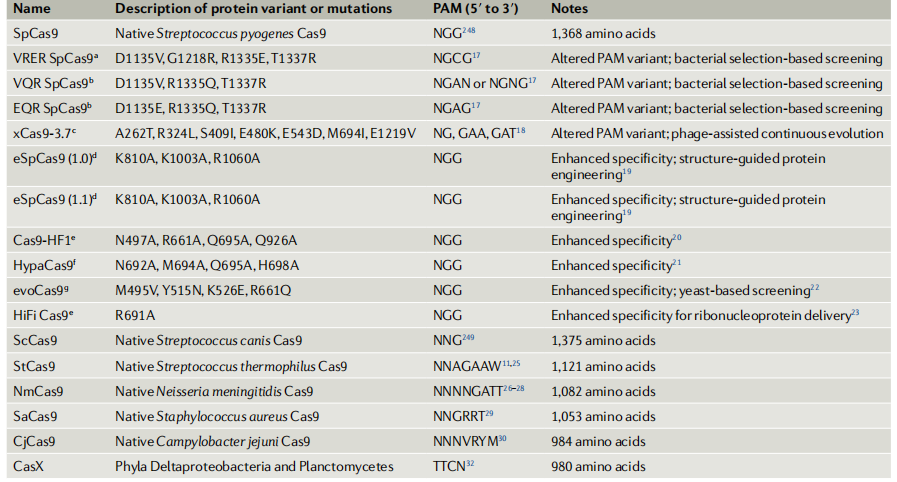
Cas9同源物的发现为识别不同PAM序列提供了更多的靶点选择。例如,嗜热链球菌Cas9可识别PAM 5ʹ-NNAGAAW (W代表A或T),而Neisseria meningitidis Cas9可识别5 ' -NNNNGATT。这些Cas9同源物已被重新用于细菌和哺乳动物细胞靶向的DNA。此外,金黄色葡萄球菌Cas9 (SaCas9)识别的PAM为5ʹ-NNGRRT (R代表A或G)。SaCas9的基因编辑效率与SpCas9相当,SaCas9的长度更小(1,053个氨基酸,SpCas9 1,368个氨基酸),使得SaCas9可以用于大小受限的载体,如腺相关病毒。最近,一个更小的Cas9同源物,来自空肠弯曲杆菌(Campylobacter jejuni,被报道识别出PAM 5ʹ-NNNVRYM (V代表A, C或G;Y代表C或T),有984个氨基酸,用于体内基因组编辑。对Cas9同源物的进一步鉴定发现了CasX(980个氨基酸),迄今为止最小的Cas9。
CRISPR-Cas12a:另一种II类RNA引导的内切酶是Cas12a,被用于人类细胞的基因编辑。Cas12a作为V型系统,在DNA目标位点上产生粘性末端。Cas12a来自Acidaminococcus spp. (AsCas12a)和Lachnospiraceae spp. (LbCas12a),这是第一个在哺乳动物细胞中被证明具有活性的Cas12a同源物,识别目标序列上游的PAM序列5ʹ-TTTV。为了增加基因组编辑活性,人们设计了AsCas12a变体(enAsCas12a)。AsCas12a变种最近被设计为识别PAMs 5ʹ-TYCV和5ʹ-TATV36或PAMs 5 ' -VTTV, 5ʹ-TTTT, 5ʹ-TTCN和5ʹ-TATV35,增加Cas12a的靶向范围。Cas12a独特的特性和剪切机制提供了一个扩展CRISPR基因组编辑工具。
Cascade和Cas3:I型系统是自然界中最常见的CRISPR-Cas系统,包括“Cascade”和内切酶Cas3(图1c)。在将Cas3招募到目标DNA序列之前,Cascade先通过PAM和间隔区识别与DNA结合。Cas3的募集产生一个单链缺口,然后通过3ʹ到5ʹ外切酶活性对目标DNA进行降解。Cas3的镍酶活性和解旋酶活性都是原核生物降解外源DNA所必需的。Cas3独特的切割机制正被利用为一种抗菌工具,将原生或外源I型系统导向细菌基因组降解和随后的细胞死亡。
2.基因组编辑机制和策略
基因编辑的机制和用途:基因编辑核酸酶,包括Cas9,通过产生靶向的DNA断裂来诱导DNA损伤反应,并通过各种内源性机制刺激修复。利用不同DNA修复机制的独特特性,可以发展特定的基因组编辑策略。
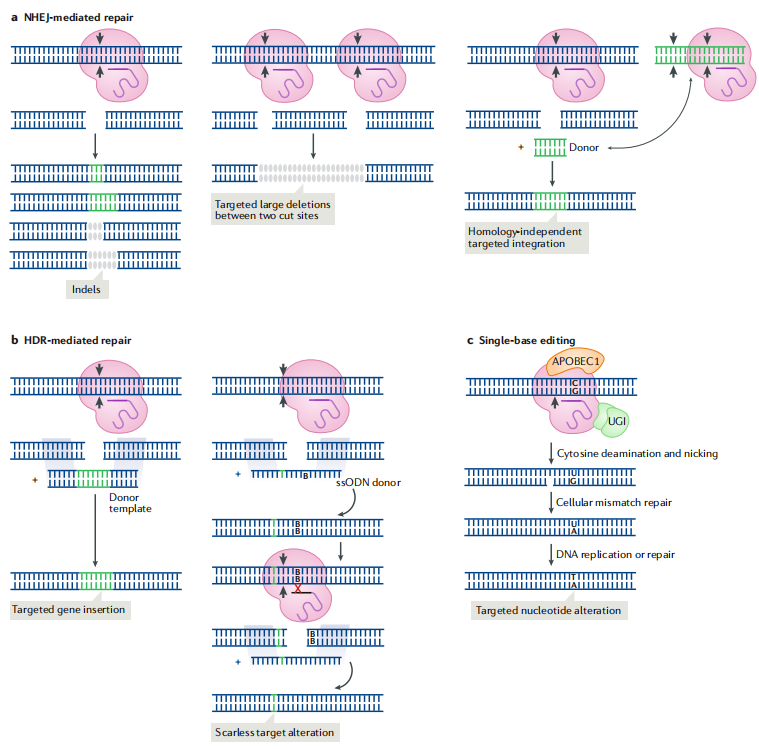
真核生物主要通过易出错的非同源末端连接(NHEJ)途径修复DSB,这导致在反复的断裂和修复周期后小插入或缺失(图2a)。另一种方法是,用Cas9与靶点同源的修复模板,以刺激无错误同源定向修复(HDR),但通常比NHEJ介导的修复效率低(图2b)。NHEJ可用于产生基因敲除,而HDR可用于引入目标基因组位点的特定变化,如点突变或插入更长的DNA片段。在Cas9裂解后,NHEJ介导的DNA修复可以敲除基因。当编码外显子时,indel介导的移码突变将破坏基因表达。或者,通过同时瞄准一个基因的两个位点,DSB之间可以产生一个缺失(图2a)。将编码标签或荧光蛋白到插入DNA序列中,以监测内源性表达的蛋白质。Cas9介导和NHEJ介导的基因编辑是基于核酸酶切割位点线性DNA片段的整合。在同源独立靶点整合中,一个标签的两侧是gRNA靶点,因此Cas9可以同时切割靶向基因相邻的受体基因组靶点(图2a)。利用非靶标特异性的通用供体序列建立内源性氨基端或羧基端基因标记融合的遗传质粒系统。HITI使用NHEJ进行DSB修复,产生了两个问题:indels的生成和供体在随机方向的整合。为了克服这些障碍,供体序列的两侧可以有同源臂。为了避免对靶特异性供体序列的分子克隆的需要,单链DNA (ssDNA)被用来用GFP编码序列标记内源性人类基因(图2b)。为了插入大的片段高效地生成条件敲除小鼠,可利用核糖核蛋白与含有短同源臂的长ssDNA。如果供体模板发生变异,包括人类多能干细胞在内的编辑细胞系可以通过致病性突变和其他的沉默突变产生,这些突变可以阻止随后的核酸酶识别靶点并形成NHEJ介导的缺失(图2b)。单碱基编辑,利用Cas9镍酶或催化缺陷的Cas9 (dCas9)进行位点特异性靶向而不产生DSB。与大鼠APOBEC1等脱氨酶融合,可以在位于间隔序列的5bp活性内实现靶向的C→T(或G→A)核苷酸转换(图2c)。细胞DNA修复反应可以拮抗这一过程并恢复编辑过的碱基。第三代编辑器(BE3)包含APOBEC1融合到16-残基XTEN连接子、Cas9 nickase和尿嘧啶糖基化酶抑制剂(APOBEC1 - XTEN - dcas9 (A840H) - ugi),可以在哺乳动物细胞中实现15-75%的目标核苷酸的转换。此外,在成年小鼠中,BE3被用于将位点特异性无义突变引入Pcsk9基因,导致胆固醇水平降低。
最近,碱基编辑已经扩展到腺嘌呤碱基编辑(ABEs),它可以进行靶向的A→G(或T→C)核苷酸转换。通过tRNA腺苷脱氨酶的定向进化和蛋白质工程开发了具有最高编辑效率和靶向活性的第7代ABE。优化增强胞苷和ABEs包括BE4max、AncBE4max和ABEmax94。随着与遗传疾病相关的已知点突变的丰富,单碱基编辑可以用作无义突变或单一氨基酸替换的动物模型。
3.RNA靶向工具及其应用
由于缺乏精确和高效的RNA靶向分子工具,靶向RNA受到限制。RNAi和反义寡核苷酸可以抑制基因表达,但需要更多的工具来研究RNA靶向作用。近年来,CRISPR-Cas结合或切割特异性RNA技术的发展,为活细胞中的RNA操作提供了先进的技术(图3)。
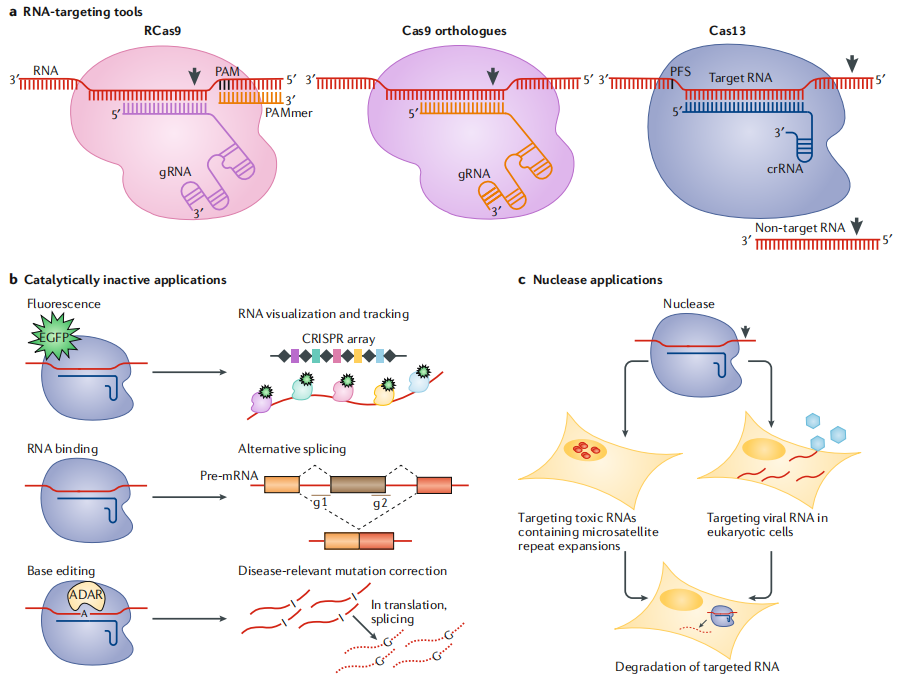
图3. RNA靶向工具及其应用
CRISPR-Cas靶向RNA的机制:Cas9可以通过提供ssDNA的PAM寡核苷酸(PAMmer)来切割ssDNA靶点。同样,PAMmer可以引导Cas9切割单链RNA (ssRNA)(图3a)。为了靶向RNA而避免DNA, PAMmers可以设计为对应基因组DNA位点上缺乏PAMs的RNA序列。这种RNA靶向Cas9系统,称为“RCas9”,只需要设计和合成一个匹配的gRNA和互补的PAMmer。通过将dCas9定位于RNA, RCas9可以作为一种RNA结合蛋白用于RNA(图3b)。该技术的进一步发展可能为低丰度或低浓度mRNA提供一个有用的工具。RCas9可以刺激ssRNA的裂解。因此,RCas9可用于在转录水平上控制细胞编辑过程。问题是DNA的脱靶效应。相比之下,RCas9的诊断和治疗潜力已通过可视化和消除与微卫星重复扩增疾病相关的有毒RNA物种得到证实(图3c)。在离体患者细胞中观察到特异性RNA靶向和消除,但体内效果仍有待证实。虽然RNA靶向疗法的发展受到不断靶向新合成转录本的需要的阻碍,但AAV可以实现基因长期表达,并且已经包装出了AAV兼容的RCas9。人们认为Cas9优先靶向细菌中的噬菌体和DNA,但Cas9同源物也有靶向RNA的能力。SaCas9以PAM不依赖的方式直接切割ssRNA (图3a)。当SaCas9靶向于RNA时,SaCas9抑制大肠杆菌中的基因表达,而对于C.空肠Cas9,显示依赖crRNA而非PAM的内源RNA的结合和切割。新Francisella novicida Cas9 (FnCas9)最初被证明是靶向细菌mRNA和改变基因表达,现已被重新用于靶向真核细胞中的丙型肝炎病毒RNA基因组。这种阳性ssRNA病毒具有细胞质生命周期,其RNA不经历逆转录和基因组整合。FnCas9通过靶向丙型肝炎病毒基因组的5个ʹ或3个ʹ非翻译区,抑制了病毒蛋白的产生和病毒复制(图3c)。与RCas9不同,FnCas9靶向的RNA是PAM独立的,因此不需要PAMmers。FnCas9还可能用于靶向阴性ssRNA病毒,如丝状病毒科、副粘病毒科和正粘病毒科。发现的Cas13 CRISPR-Cas系统含有天然RNA靶向内切酶。在细菌中,Cas13a是一种RNA靶向核酸酶。这种2类VI型CRISPR蛋白在识别ssRNA靶蛋白时被激活(图3a)。Cas13a在邻近的尿嘧啶碱基上剪切,这种“附带”剪切也延伸到附近的非靶向RNA。通过将dCas13融合到作用于RNA的腺苷脱氨酶上,开发了一种单碱基编辑RNA(图3b)。这个系统被称为“REPAIR”,可以在真核细胞中进行腺苷到肌苷的编辑。通过对细菌基因组测序,发现了一种ii类 CRISPRCas,称为“Cas13d”。与Cas13类似,Cas13d对RNA的识别是PFS独立的。Cas13已被用于在额颞叶痴呆的神经元模型中靶向mRNA顺式元件的crRNA来操纵选择性剪接(图3b)。
4.靶向基因调控等应用
除了通过形成DNA断裂来编辑基因外,可通过Cas9作为DNA识别复合体而非靶向核酸酶来实现位点特异性基因调控。RuvC (D10A)和HNH (H840A)核酸酶结构域的突变破坏了Cas9的催化活性,同时保持其RNA引导的DNA靶向能力。CRISPR-Cas已经通过将该dCas9与多种效应因子(如转录抑制因子或激活因子、表观遗传修饰因子和荧光团)融合(图4)。
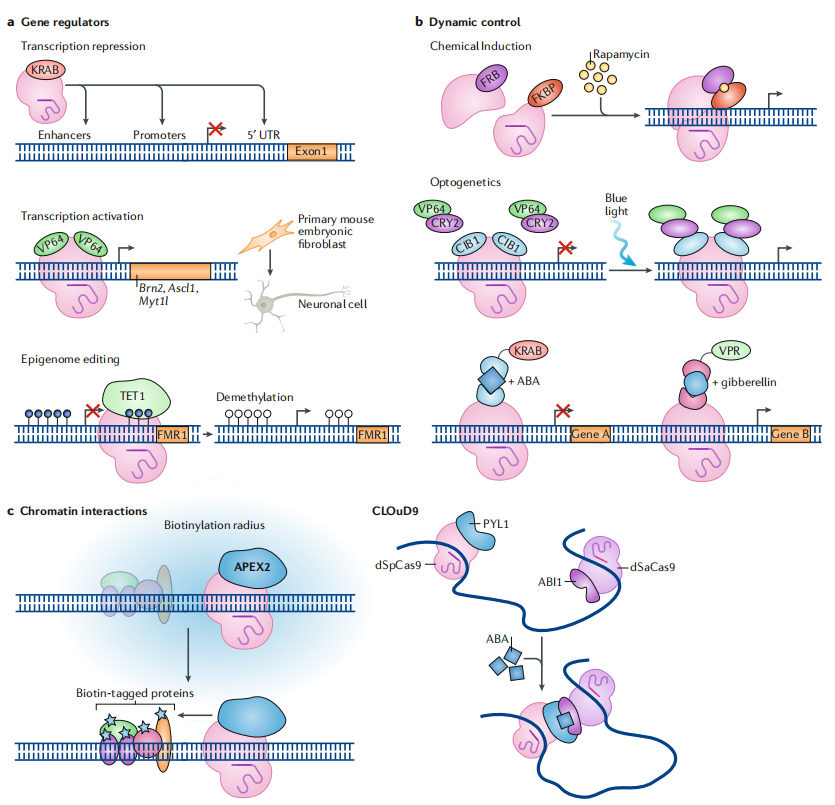
图4. 靶向基因调控等应用
CRISPR干扰:dCas9与DNA元件的结合可能通过空间阻碍RNA聚合酶机制来抑制转录。dcas9介导干扰,称为“CRISPR干扰”(CRISPRi),在原核细胞中有效,但在真核细胞中效果较差。为了提高CRISPR在真核细胞中的抑制能力,研究人员将dCas9与转录抑制因子结构域(如Krüppel-associated box (KRAB))相连,该结构域在许多天然锌指转录因子中都存在。已知KRAB可以诱导异染色质的形成,染色质结构的变化通常伴随着dCas9 - KRAB靶向的转录抑制。dCas9-KRAB在哺乳动物细胞中是一个强大的工具,它可以通过靶向启动子区域、5ʹ非翻译区域和近端和远端增强子元件(图4a),有效地沉默单基因和非编码RNA。dCas9-KRAB的多功能性是通过靶向基因和基因调控区域来抑制转录。
CRISPR激活:dCas9也可以融合为程序化转录激活的激活子,称为“CRISPR激活”(CRISPRa)。在真核生物中,报告基因和内源性基因都可以被融合到核因子-κB反转录激活亚基(p65)的转录激活域或VP64的dCas9激活。通过将多个gRNAs靶向到一个启动子区域,这些合成转录因子协同基因激活。此外,还可以通过组合不同的激活域来实现协同作用。例如,直接转换基本实现了小鼠胚胎成纤维细胞诱导神经细胞激活后通过VP64-dCas9-VP64 (dCas9融合在它的每个末端VP64)的内源性Brn2(也称为Pou3f2), Ascl1和Myt1l genes(图4),类似的方法也已被应用于将细胞重编程成多能性细胞或成肌细胞。Cas9功能的动态控制诱导系统的功能需要特定的刺激基因激活。根据刺激类型的不同,人们开发了各种策略来生成可诱导的Cas9-based系统,对cas9介导的基因靶向进行控制(图4b)。
化学感应:化合物可以通过诱导启动子激活Cas9的表达。这可能是希望精确敲除某些细胞类型,而不是使用组成敲除细胞系。多西环素诱导Cas9表达已用于人类多能干细胞和成年小鼠。然而,在转染的细胞中观察到霉素的突变,这表明在这些系统中Cas9的表达存在漏洞。基于诱导dcas9的系统也在表观基因组工程中提供多功能性。CRISPRi系统在诱导的多能干细胞来源的心肌细胞中进行高效、可调节和可逆的疾病建模。化学诱导CRISPRa系统使用条件稳定的dCas9激活剂和化学诱导后二聚的分裂dCas9激活剂(图4b)。
光遗传学:光诱导dCas9系统内源基因的调控。如植物源细胞色素CRY2与其结合伙伴CIB1的光诱导二聚已被用于生成光激活的dCas9-p65和dCas9-VP64 (图4b)。通过将燕麦(Avena sativa)的光传感器与SpCas9抑制剂配对,构建了一种抗CRISPR蛋白,用于人类细胞中基因组和表观基因组的光介导调控。我们开发了第二代光遗传分裂蛋白系统,目的是上调NEUROD1基因的表达以诱导神经元诱导多能干细胞的分化,多种化学诱导和光诱导系统已被用于动态操纵多个基因的激活或抑制(图4b)。这些光诱导系统有希望实现建模发展和时间控制的基因表达。

将CRISPR-Cas系统重新应用于真核细胞已经彻底改变了基因组工程领域。即使II型CRISPR-Cas系统的广泛使用,来自原核物种的CRISPR系统的不断发现和发展也带来了新的技术,如基于Cas13的RNA靶向工具,将dCas9与众多效应器融合将继续扩大靶向表观遗传调制。用于大规模Cas9靶向的gRNA文库,加上NGS技术的进步,使得全基因组遗传和表观遗传筛选变得容易。随着基于CRISPR-Cas技术进入临床测试,在纠正遗传疾病和增强细胞治疗方面具有巨大的潜力。临床前结果是有希望的,但安全性和有效性需要在这些研究期间密切监测。使用基因编辑方法的一个潜在风险是将偏离靶标的变化引入基因组序列,因此改进检测罕见突变的方法并量化其潜在风险对未来的临床进展非常重要。
擎科可提供:
1.擎科可承接各种类型动物细胞,细菌,真菌的敲入/敲除实验;
2.更多CRISPi和CRISPa质粒产品类型:
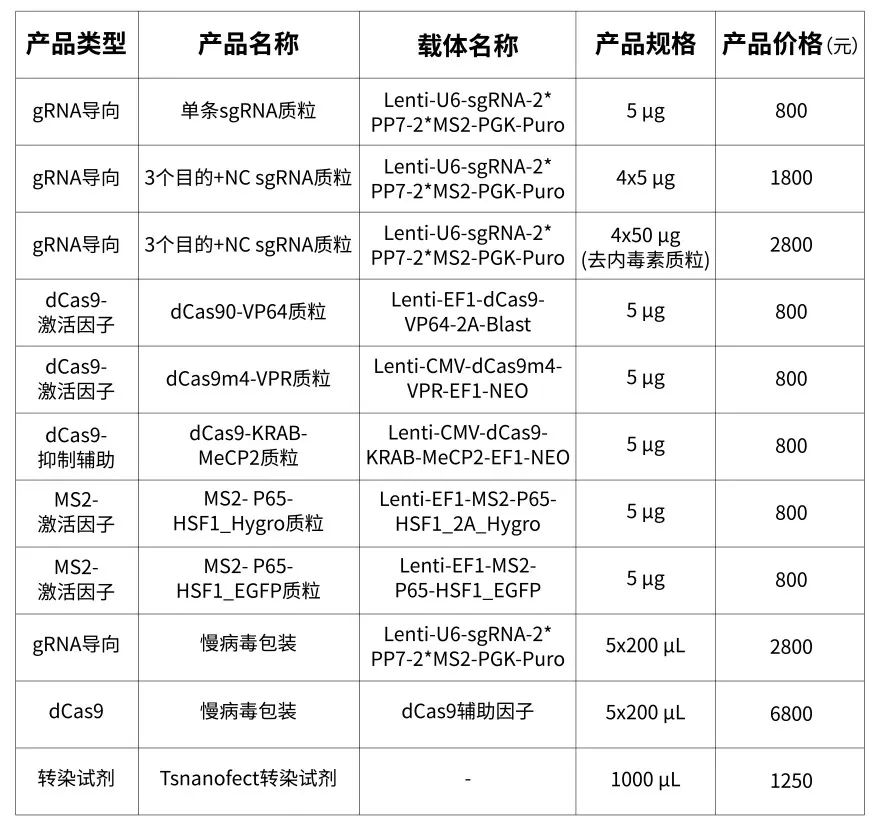
回复小编或联系service@tsingke.com.cn即刻开聊,下单可直接联系当地销售经理。
参考文献:
[1]Adrian Pickar-Oliver, Charles A. Gersbach , etal. The next generation of CRISPR–Cas technologies and applications.Nature Reviews Molecular Cell Biology,2019.







